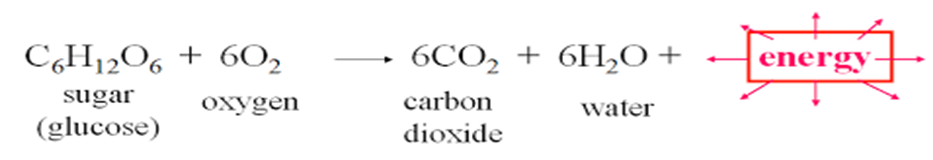kompetensi 7
indikator 24 : menjelaskan ciri & cara dari faktor yang mempengaruhi kerja enzim
Enzim merupakan protein yang bertindak sebagai katalis. Di dalam tubuh organisme, enzim befungsi sebagai biokatalisator. Berdasarkan komponen penyusunnya, enzim dibedakan menjadi dua yaitu enzim sederhana dan enzim kompleks. Enzim sederhana hanya terdiri dari protein. Sedangkan, enzim kompleks terdiri atas apoenzim (komponen protein) dan gugus prostetik (komponen nonprotein).
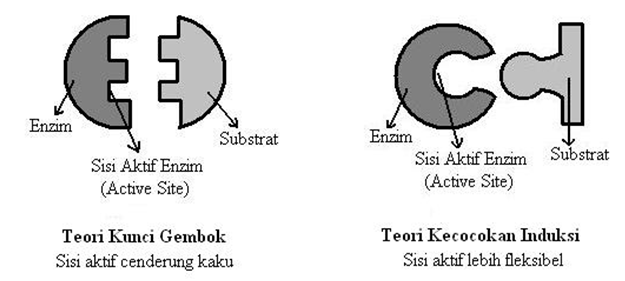
Enzim terdiri atas sisi aktif dan sisi alosterik. Substrat akan berikatan dengan enzim pada sisi aktifnya. Mekanisme kerja enzim diterangkan dengan kedua teori, yaitu teori gembok dan kunci serta teori ketepatan induksi. Berdasarkan prinsip teori gembok dan kunci, sisi aktif enzim hanya dapat berikatan dengan substrat yang sesuai. Sementara itu, dalam teori ketepatan induksi, sisi aktif enzim akan menyesuaikan dengan bentuk substrat yang akan berikatan dengan enzim tersebut.
Enzim memiliki sifat-sifat sebagai berikut:
1. Enzim bekerja spesifik. Artinya, enzim hanya bekerja pada substrat-substrat tertentu saja.
2. Enzim bersifat termolabil. Artinya, kerja enzim dipengaruhi oleh suhu. Enzim tidak aktif pada suhu rendah dan akan rusak pada suhu tinggi.
3. Enzim dapat bekerja secara bolak-balik (reversible). Artinya enzim hanya mempercepat laju reaksi sampai terjadi kesetimbangan.
4. Enzim dapat bereaksi baik dengan substrat asam maupun basa. Pada sisi aktif enzim terdapat gugus R residu asam amino yang membuat enzim dapat beraksi dengan substrat asam maupun basa.
5. Enzim merupakan koloid. Dengan demikian, enzim dapat memperluas permukaannya sehingga aktivitasnya semakin besar.
6. Enzim merupakan biokatalisator. Enzim dalam jumlah yang sedikit sudah dapat mempercepat reaksi. Enzim tidak ikut bereaksi.
Dalam tugasnya mempercepat suatu reaksi biologi dalam tubuh, enzim dipengaruhi oleh beberapa faktor sebagai berikut:
1. Suhu
Enzim dapat bekerja secara optimum pada kisaran suhu 38-40. Jika suhu terlalu rendah maka enzim akan inaktif atau tidak akan bekerja. Namun, pada suhu di atas suhu optimum enzim akan mengalami denaturasi atau kerusakan.
2. Derajat Keasaman (pH)
Enzim memiliki pH optimum yang dapat bersifat basa maupun asam. Misalnya, enzim renin yang bekerja optimum pada pH asam, enzim maltase yang bekerja optimum pada pH basa, dan enzim ptialin yang bekerja pada pH netral. Sebagian besar enzim memiliki pH optimum antara 6-8. Perubahan pH dapat mengakibatkan sisi aktif enzim berubah keefektifannya dalam membentuk kompleks enzim-substrat. Perubahan pH juga dapat menyebabkan enzim terdenaturasi.
3. Konsentrasi Enzim
Konsentrasi enzim berbanding lurus dengan kecepatan reaksi. Jadi, penambahan konsentrasi enzim dapat meningkatkan kecepatan reaksi hingga tercapai kecepatan konstan. Kecepatan konstan tercapai apabila semua substrat sudah terikat oleh enzim.
4. Konsentrasi Substrat
Kecepatan reaksi akan meningkat dengan adanya penambahan konsetrasi substrat meskipun konsentrasi enzim tetap. Namun demikian, ketika semua sisi aktif enzim sedang bekerja, penambahan konsentrasi substrat tidak dapat meningkatkan kecepatan reaksi. Keadaan seperti ini menunjukkan kecepatan reaksi telah mencapai titik maksimum.
5. Zat Penghambat (Inhibitor)
Inhibitor merupakan suatu molekul yang dapat menghambat aktivitas enzim. Ada dua macam inhibitor, yaitu inhibitor kompetitif dan inhibitor nonkompetitif. Inhibitor kompetitif adalah molekul penghambat kerja enzim yang bekerja dengna cara bersaing dengan substrat untuk berikatan dengan sisi aktif enzim. Inhibitor kompetitif memiliki struktur yang sama dengan substrat. Pada saat inhibitor kompetitif berikatan dengan sisi aktif enzim maka substrat sudah tidak dapat berikatan dengan enzim tersebut. Contohnya, sianida bersaing dengan oksigen untuk berikatan dengan hemoglobin.
Inhibitor nonkompetitif adalah molekul penghambat kerja enzim yang bekerja dengan cara melekatkan diri pada luar sisi aktif enzim (sisi alosterik) yang dapat menyebabkan sisi aktif enzim berubah dan tidak dapat berfungsi lagi.
6. Zat Penggiat (Aktivator)
Zat aktivator adalah zat yang dapat meningkatkan aktivitas enzim. Atau dengan kata lain, aktivator merupakan molekul yang mempermudah ikatan antara enzim dengan substrat. Contohnya, garam-garam dari logam alkali dalam kondisi encer dapat memicu aktivitas enzim.
Enzim terdiri atas sisi aktif dan sisi alosterik. Substrat akan berikatan dengan enzim pada sisi aktifnya. Mekanisme kerja enzim diterangkan dengan kedua teori, yaitu teori gembok dan kunci serta teori ketepatan induksi. Berdasarkan prinsip teori gembok dan kunci, sisi aktif enzim hanya dapat berikatan dengan substrat yang sesuai. Sementara itu, dalam teori ketepatan induksi, sisi aktif enzim akan menyesuaikan dengan bentuk substrat yang akan berikatan dengan enzim tersebut.
Enzim memiliki sifat-sifat sebagai berikut:
1. Enzim bekerja spesifik. Artinya, enzim hanya bekerja pada substrat-substrat tertentu saja.
2. Enzim bersifat termolabil. Artinya, kerja enzim dipengaruhi oleh suhu. Enzim tidak aktif pada suhu rendah dan akan rusak pada suhu tinggi.
3. Enzim dapat bekerja secara bolak-balik (reversible). Artinya enzim hanya mempercepat laju reaksi sampai terjadi kesetimbangan.
4. Enzim dapat bereaksi baik dengan substrat asam maupun basa. Pada sisi aktif enzim terdapat gugus R residu asam amino yang membuat enzim dapat beraksi dengan substrat asam maupun basa.
5. Enzim merupakan koloid. Dengan demikian, enzim dapat memperluas permukaannya sehingga aktivitasnya semakin besar.
6. Enzim merupakan biokatalisator. Enzim dalam jumlah yang sedikit sudah dapat mempercepat reaksi. Enzim tidak ikut bereaksi.
Dalam tugasnya mempercepat suatu reaksi biologi dalam tubuh, enzim dipengaruhi oleh beberapa faktor sebagai berikut:
1. Suhu
Enzim dapat bekerja secara optimum pada kisaran suhu 38-40. Jika suhu terlalu rendah maka enzim akan inaktif atau tidak akan bekerja. Namun, pada suhu di atas suhu optimum enzim akan mengalami denaturasi atau kerusakan.
2. Derajat Keasaman (pH)
Enzim memiliki pH optimum yang dapat bersifat basa maupun asam. Misalnya, enzim renin yang bekerja optimum pada pH asam, enzim maltase yang bekerja optimum pada pH basa, dan enzim ptialin yang bekerja pada pH netral. Sebagian besar enzim memiliki pH optimum antara 6-8. Perubahan pH dapat mengakibatkan sisi aktif enzim berubah keefektifannya dalam membentuk kompleks enzim-substrat. Perubahan pH juga dapat menyebabkan enzim terdenaturasi.
3. Konsentrasi Enzim
Konsentrasi enzim berbanding lurus dengan kecepatan reaksi. Jadi, penambahan konsentrasi enzim dapat meningkatkan kecepatan reaksi hingga tercapai kecepatan konstan. Kecepatan konstan tercapai apabila semua substrat sudah terikat oleh enzim.
4. Konsentrasi Substrat
Kecepatan reaksi akan meningkat dengan adanya penambahan konsetrasi substrat meskipun konsentrasi enzim tetap. Namun demikian, ketika semua sisi aktif enzim sedang bekerja, penambahan konsentrasi substrat tidak dapat meningkatkan kecepatan reaksi. Keadaan seperti ini menunjukkan kecepatan reaksi telah mencapai titik maksimum.
5. Zat Penghambat (Inhibitor)
Inhibitor merupakan suatu molekul yang dapat menghambat aktivitas enzim. Ada dua macam inhibitor, yaitu inhibitor kompetitif dan inhibitor nonkompetitif. Inhibitor kompetitif adalah molekul penghambat kerja enzim yang bekerja dengna cara bersaing dengan substrat untuk berikatan dengan sisi aktif enzim. Inhibitor kompetitif memiliki struktur yang sama dengan substrat. Pada saat inhibitor kompetitif berikatan dengan sisi aktif enzim maka substrat sudah tidak dapat berikatan dengan enzim tersebut. Contohnya, sianida bersaing dengan oksigen untuk berikatan dengan hemoglobin.
Inhibitor nonkompetitif adalah molekul penghambat kerja enzim yang bekerja dengan cara melekatkan diri pada luar sisi aktif enzim (sisi alosterik) yang dapat menyebabkan sisi aktif enzim berubah dan tidak dapat berfungsi lagi.
6. Zat Penggiat (Aktivator)
Zat aktivator adalah zat yang dapat meningkatkan aktivitas enzim. Atau dengan kata lain, aktivator merupakan molekul yang mempermudah ikatan antara enzim dengan substrat. Contohnya, garam-garam dari logam alkali dalam kondisi encer dapat memicu aktivitas enzim.
indikator 25 : menjelaskan proses katabolisme karbohidrat
Respirasi merupakan proses reduksi, oksidasi, dan dekomposisi dari senyawa organic kompleks menjadi senyawa yang lebih sederhana dengan memlepaskan beberapa energi. Ada 2 (dua) macam respirasi, yaitu respirasi aerob dan respirasi anaerob. Respirasi yang menggunakan oksigen adalah respirasi aerob.
Reaksi aerob emiliki 4 (empat) tahap, yaitu glikolisis (katabolisme karbohidrat), pembentukan asetil Ko-A, siklus krebs dan system tranpor electron.
Reaksi kimia pada respirasi aerob berupa berikut:
Reaksi aerob emiliki 4 (empat) tahap, yaitu glikolisis (katabolisme karbohidrat), pembentukan asetil Ko-A, siklus krebs dan system tranpor electron.
Reaksi kimia pada respirasi aerob berupa berikut:
1. Glikolisis
Glikolisis berlangsung didalam sitoplasma. Glikolisis merupakan pemecahan dari molekul glukosa (C6) menjadi asam piruvat (C3). Didalam proses glikolisis mengahasilkan 2 asam piruvat dan 2 ATP. Lalu masuk ketahap berikutnya.
(bersambung)
Glikolisis berlangsung didalam sitoplasma. Glikolisis merupakan pemecahan dari molekul glukosa (C6) menjadi asam piruvat (C3). Didalam proses glikolisis mengahasilkan 2 asam piruvat dan 2 ATP. Lalu masuk ketahap berikutnya.
(bersambung)
indikator 26 : menjelaskan zat yang dihasilkan pada proses respirasi aerob
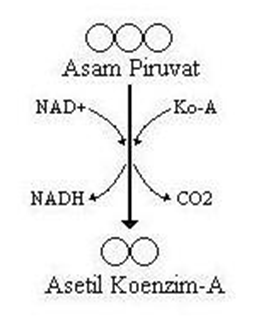
2. Deokarboksilasi oksidatif (lanjutan)
Proses ini berlangsung didalam mitokondria. Setiap asam purivat yang dihasilkan dari proses glikolisis akan diberaksi dengan NAD+ dan Koenzim A mengahasilkan Asetil Ko-A. didalam proses ini terjadi pengurangan satu atom C dalam bentuk CO2.
3. Siklus Krebs
Siklus Krebs terjadi di dalam mitokondria. Selama reaksi siklus Krebs dilepaskan 2 molekul karbon dioksida, 3 NADH, 1 FADH2, dan 1 ATP. Reaksi ini terjadi dua kali karena pada proses glikolisis gula telah dipecah menjadi 2 molekul asam piruvat, sehingga akhir dari Siklus Krebs akan menghasilkan 4 CO2, 6 NADH, 2 FADH2, dan 2 ATP.
Siklus Krebs terjadi di dalam mitokondria. Selama reaksi siklus Krebs dilepaskan 2 molekul karbon dioksida, 3 NADH, 1 FADH2, dan 1 ATP. Reaksi ini terjadi dua kali karena pada proses glikolisis gula telah dipecah menjadi 2 molekul asam piruvat, sehingga akhir dari Siklus Krebs akan menghasilkan 4 CO2, 6 NADH, 2 FADH2, dan 2 ATP.
4. Transport electron
Transpor elektron berlangsung pada krista mitokondria. Prinsip dari reaksi ini adalah setiap pemindahan ion H (elektron) yang dilepas dari dua langkah pertama tadi antar akseptor dihasilkan energi yang digunakan untuk pembentukan ATP.
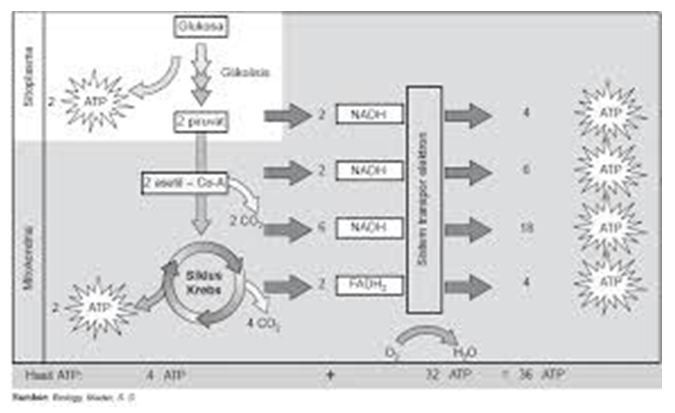
Keempat tahapan berikut dapat dilihat pada bagian berikut:
Transpor elektron berlangsung pada krista mitokondria. Prinsip dari reaksi ini adalah setiap pemindahan ion H (elektron) yang dilepas dari dua langkah pertama tadi antar akseptor dihasilkan energi yang digunakan untuk pembentukan ATP.
Keempat tahapan berikut dapat dilihat pada bagian berikut:
indikator 27 : menjelaskan tahapan proses anabolisme (fotosintesis) pada tumbuhan
Iya, iya. Gue tahu, judul asli dari SKL-nya itu anabolisme. Tapi kita semua mengenalnya sebagai fotosintesis, kan? *kedip mata*
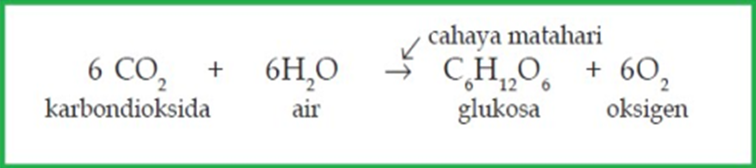
Well, kalau tadi kita mengenal katabolisme sebagai proses memecah (dari glukosa menjadi partikel lebih kecil), maka anabolisme adalah menggabungkan partikel yang lebih kecil (dalam hal ini karbon dioksida) menjadi partikel besar (glukosa). Lalu, kalau anabolisme itu hanya menggabungkan partikel, mengapa masih butuh cahaya?
Oke, jadi perlu diingat kalau fotosintesis terdiri dari dua bagian utama: reaksi terang (yang butuh cahaya, nama lainnya fotofosforilasi) dan reaksi gelap (alias siklus Calvin). Reaksi terang berfungsi untuk menyiapkan energi yang dipakai untuk menggabungkan para partikel di reaksi gelap.
Eh, anyway, kalian masih ingat kan, komponen utama fotosintesis? Ingat ya, karbon dioksida dipakai di reaksi gelap dan letaknya ada di stroma, sementara air dipakai di reaksi terang yang letaknya di membran tilakoid.
Well, kalau tadi kita mengenal katabolisme sebagai proses memecah (dari glukosa menjadi partikel lebih kecil), maka anabolisme adalah menggabungkan partikel yang lebih kecil (dalam hal ini karbon dioksida) menjadi partikel besar (glukosa). Lalu, kalau anabolisme itu hanya menggabungkan partikel, mengapa masih butuh cahaya?
Oke, jadi perlu diingat kalau fotosintesis terdiri dari dua bagian utama: reaksi terang (yang butuh cahaya, nama lainnya fotofosforilasi) dan reaksi gelap (alias siklus Calvin). Reaksi terang berfungsi untuk menyiapkan energi yang dipakai untuk menggabungkan para partikel di reaksi gelap.
Eh, anyway, kalian masih ingat kan, komponen utama fotosintesis? Ingat ya, karbon dioksida dipakai di reaksi gelap dan letaknya ada di stroma, sementara air dipakai di reaksi terang yang letaknya di membran tilakoid.
A. Reaksi Terang
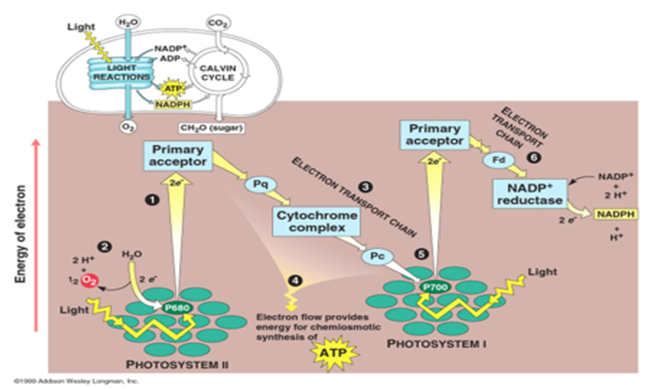
Pertama, sebelum memahami gambar di atas, kita perlu paham dulu: gambar di atas itu maksudnya apa sih? Pada dasarnya, di membran tilakoid, ada dua jenis fotosistem yang tugasnya mengumpulkan cahaya dan terdiri dari kumpulan molekul pigmen. Fotosistem tersebut adalah fotosistem 1 (dia menerima cahaya yang panjang gelombangnya 700 nm) dan fotosistem 2 (menerima cahaya dengan panjang gelombang 680 nm--kalau kalian kepo, keduanya adalah cahaya berwarna merah). Selain itu, ada kompleks sitokrom, dan cara kerjanya mirip dengan transpor elektron: membentuk ATP dari ADP dan NADPH dari NADP!
Fotofosforilasi terbagi menjadi dua: siklik dan non-siklik
1. Fotofosforilasi non-siklik
Fotofosforilasi non-siklik dimulai ketika molekul air di fotosistem 2 dipecah oleh foton (partikel yang ada pada cahaya matahari) menjadi hidrogen, oksigen, dan elektron.
Oksigen dilepas ke udara bebas, hidrogen dipakai untuk membuat NADPH, sementara elektron yang ada menyebabkan para pigmen molekul tidak seimbang. Akibatnya, elektron melompat-lompat (lebih tepatnya, tereksitasi agar level energinya bertambah) antar pigmen molekul hingga mencapai pusat penerimaan elektron (akseptor primer).
Dari akseptor primer, elektron melompat ke rantai transpor elektron, melewati plastokuinon, kompleks sitokrom, danplastosianin. Aliran elektron ini menghasilkan energi besar yang dapat mengubah ADP menjadi ATP. Halo, energi!
Elektron yang selesai mengalir masuk ke fotosistem 1, dan melompat lagi hingga mencapai akseptor primer. Setelah itu, elektron masuk ke rantai transpor elektron lainnya yang terdiri dari ferodoksin dan NADP+ reduktase, mengubah NADP+ menjadiNADPH dengan hidrogen hasil pemecahan air dan elektron yang tersisa.
2. Fotofosforilasi siklik
Proses yang satu ini hanya berkaitan dengan fotosistem 1. Foton yang mencapai fotosistem 1 menyebabkan lompatan elektron hingga ke akseptor primer dan ferodoksin. Namun bukannya pergi ke NADP+ reduktase, elektron malah pergi ke plastokuinon, sehingga masuk ke rantai transpor elektron yang menghasilkan ATP.
B. Reaksi Gelap (Siklus Calvin)
Fotofosforilasi terbagi menjadi dua: siklik dan non-siklik
1. Fotofosforilasi non-siklik
Fotofosforilasi non-siklik dimulai ketika molekul air di fotosistem 2 dipecah oleh foton (partikel yang ada pada cahaya matahari) menjadi hidrogen, oksigen, dan elektron.
Oksigen dilepas ke udara bebas, hidrogen dipakai untuk membuat NADPH, sementara elektron yang ada menyebabkan para pigmen molekul tidak seimbang. Akibatnya, elektron melompat-lompat (lebih tepatnya, tereksitasi agar level energinya bertambah) antar pigmen molekul hingga mencapai pusat penerimaan elektron (akseptor primer).
Dari akseptor primer, elektron melompat ke rantai transpor elektron, melewati plastokuinon, kompleks sitokrom, danplastosianin. Aliran elektron ini menghasilkan energi besar yang dapat mengubah ADP menjadi ATP. Halo, energi!
Elektron yang selesai mengalir masuk ke fotosistem 1, dan melompat lagi hingga mencapai akseptor primer. Setelah itu, elektron masuk ke rantai transpor elektron lainnya yang terdiri dari ferodoksin dan NADP+ reduktase, mengubah NADP+ menjadiNADPH dengan hidrogen hasil pemecahan air dan elektron yang tersisa.
2. Fotofosforilasi siklik
Proses yang satu ini hanya berkaitan dengan fotosistem 1. Foton yang mencapai fotosistem 1 menyebabkan lompatan elektron hingga ke akseptor primer dan ferodoksin. Namun bukannya pergi ke NADP+ reduktase, elektron malah pergi ke plastokuinon, sehingga masuk ke rantai transpor elektron yang menghasilkan ATP.
B. Reaksi Gelap (Siklus Calvin)
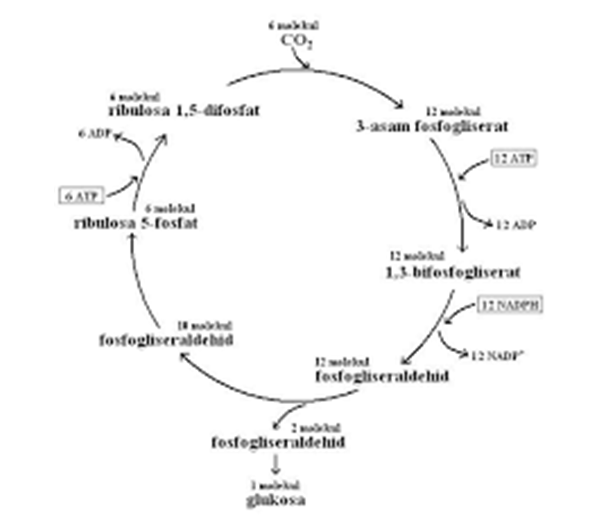
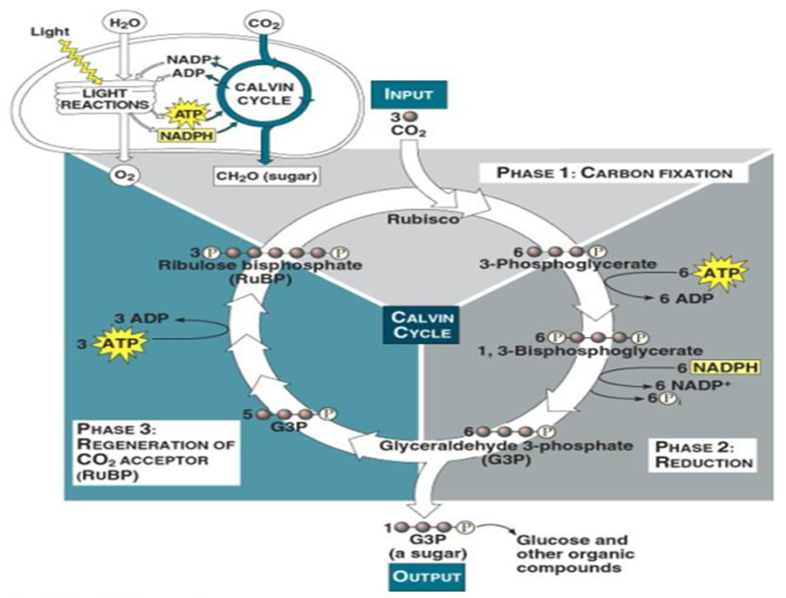
Sekarang kita masuk dalam pembuatan energi! Untuk membuat satu molekul glukosa, dibutuhkan 6 CO2, 24 ATP, dan 12 NADPH. Ada tiga fase dalam siklus Calvin, yakni fiksasi, reduksi, dan regenerasi.
· Fiksasi
Di sini, karbon dioksida ditempelkan (fiksasi) pada ribulosa difosfat (RuBP) menggunakan enzim rubisco. Namun karena tidak stabil, molekul ini langsung pecah menjadi 3-fosfogliserat yang memiliki tiga karbon. Penambahan gugus fosfat menyebabkan 3-fosfogliserat berubah menjadi 1,3-difosfogliserat dan perubahan dari ATP menjadi ADP.
· Reduksi
Gugus fosfat ini akan dicabut kembali, menggunakan energi dari perubahan NADPH menjadi NADP+ sehingga berubah menjadi 3-fosfogliseraldehida (PGAL).
Masih ingat kan, kalau kita punya 12 PGAL? Dua di antaranya akan dijadikan glukosa, sementara sepuluh sisanya akan masuk ke proses selanjutnya.
· Regenerasi
Dengan bantuan enzim yang sangat kompleks, sepuluh PGAL yang tersisa diubah kembali menjadi 6 RuBP. Selain itu, dibutuhkan pula 12 ATP yang diubah menjadi ADP untuk mendapatkan gugus fosfat yang dibutuhkan oleh RuBP.
· Fiksasi
Di sini, karbon dioksida ditempelkan (fiksasi) pada ribulosa difosfat (RuBP) menggunakan enzim rubisco. Namun karena tidak stabil, molekul ini langsung pecah menjadi 3-fosfogliserat yang memiliki tiga karbon. Penambahan gugus fosfat menyebabkan 3-fosfogliserat berubah menjadi 1,3-difosfogliserat dan perubahan dari ATP menjadi ADP.
· Reduksi
Gugus fosfat ini akan dicabut kembali, menggunakan energi dari perubahan NADPH menjadi NADP+ sehingga berubah menjadi 3-fosfogliseraldehida (PGAL).
Masih ingat kan, kalau kita punya 12 PGAL? Dua di antaranya akan dijadikan glukosa, sementara sepuluh sisanya akan masuk ke proses selanjutnya.
· Regenerasi
Dengan bantuan enzim yang sangat kompleks, sepuluh PGAL yang tersisa diubah kembali menjadi 6 RuBP. Selain itu, dibutuhkan pula 12 ATP yang diubah menjadi ADP untuk mendapatkan gugus fosfat yang dibutuhkan oleh RuBP.
indikator 28 : menjelaskan proses kemosintesis/respirasi anaerob
Teori
Respirasi Anaerob merupakan respirasi yang tidak menggunakan oksigen. Respirasi anaerob juga menggunakan glukosa sebagai substrat. Respirasi anaerob merupakan proses fermentasi yang terjadi pada sitoplasma. Fermentasi juga dibedakan menjadi fermentasi alcohol dan fermentasi asam laktat.
1. Fermentasi Alkohol
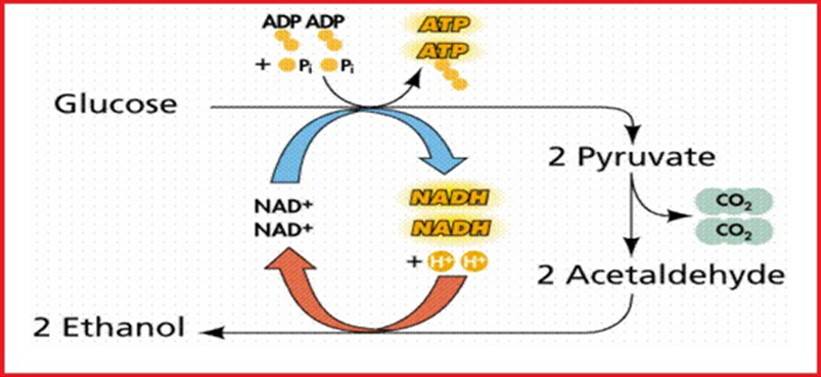
Fermentasi alcohol dilakukan oleh jamur ragi (yeast) secara anaerob. Reaksinya adalah:
Fermentasi Alkohol terjadi pada proses pembuatan tapai dan anggur.
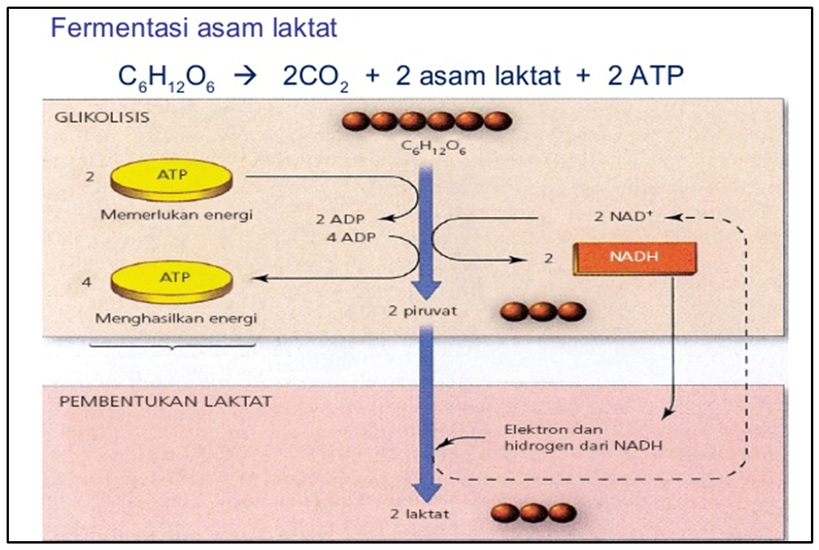
2. Fermentasi Asam Laktat
Fermentasi Asam Laktat terjadi pada otot manusia saat melakukan kerja keras dan persediaan oksigen kurang mencukupi.
Reaksi fermentasi asam laktat sebagai berikut:
2. Fermentasi Asam Laktat
Fermentasi Asam Laktat terjadi pada otot manusia saat melakukan kerja keras dan persediaan oksigen kurang mencukupi.
Reaksi fermentasi asam laktat sebagai berikut:
Respirasi anaerob menghasil energy yang lebih sedikit dibandingkan dengan respirasi aerob. ATP yang dihasilkan respirasi aerob adalah 36 ATP untuk oksidasi satu molekul glukosa. Sementara itu, fermentasi satu molekul glukosa hanya menghasilkan 2 ATP. Hal ini dikarenakan respirasi aerob merupakan katabolisme sempurna yang menghasilkan CO2 dan H2O. Jadi, pembakaran yang dihasilkan lebih optimum. Sebaliknya, hasil fermentasi berupa senyawa karbon yang masih reduktif, misal etanol dan asam laktat. Oleh karena itu, etanol masih mengandung energy terikat yang masih dapat dibakar untuk menghasilkan energy lanjutan.